合格の60点以上を取るために必要最低限絞り込んだ学習ポイントと問題を盛り込んだ試験対策サイトです!
It is the exam site that incorporates the problem and learning point narrowed down the minimum required to take 60 or more points pass!
このサイトは日本国家資格の「危険物取扱者」の受験対策について記載されています。資格試験の出題箇所について独自の分析により、必要最小限の内容となっております。
This site is a national qualification in Japan, "Hazardous materials engineer" are described for exam measures. The point for your own analysis of exam questions, and ordered the contents of the minimum.
リンクや広告について
当サイトには広告や別サイトへのリンクがありますので、ご確認ください。また配信事業者はCookieを使用してウェブサイト閲覧履歴に基づく広告を配信しております。
危険物取扱者に必要な基礎化学 物質の基本と化学変化1
物質の基本と化学変化
物質には物理変化と化学変化の二つの変化があります。
すでに基礎物理のページを学習された方は、物質の三態について理解されていると思います。
それらは物理変化と言い、状態や形が変化するだけの変化です。(簡単に元に戻る変化です)
念のため、例を挙げておきます。
- 水が水蒸気になる。
- ニクロム線に電気を流すと赤熱する。
- 金属が溶ける。
※ 上記3つは物理変化です。必ず覚えておきましょう。
では、基礎化学のページで学習する変化とは何なのかを説明してゆきます。
化学変化
物質の性質が変化したり、別の物質になる変化のことをいいます。(簡単に元に戻らない変化)
- 鉄がさびた。
- 濃硫酸に紙をつけると黒く変色した。
- ガソリンが燃えて二酸化炭素と水蒸気が出来た。
- 水を電気分解で水素と酸素に分けた。
※ 上記4つは化学変化です。必ず覚えておきましょう。
電気分解の実験は中学校?でやっていると思います。水に電極を入れて直流電気を流すと、プラスの電極には酸素が、マイナスの電極には水素が発生します。水はH2Oですから、水素が2つと酸素が1つの化合物です。そのため、水が分解されると水素は酸素の2倍発生します。
さて、発生した水素や酸素は分子といわれるもので、化学用語では単体と言われています。
これらの物質の造りについて少し勉強しましょう。
原子と分子
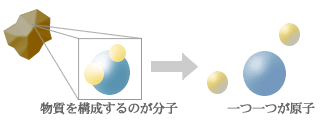 左の図を見ていただくとわかると思いますが、物質は分子で出来ていて、その分子は原子の集まりです。
左の図を見ていただくとわかると思いますが、物質は分子で出来ていて、その分子は原子の集まりです。
現代では原子がさらに陽子や電子などから出来ていて、素粒子と呼ばれたりしています。それらの粒子は最小の単位とされていて、物質的な大きさを持たないと言われています。
とりあえず、先端化学における物質の仕組みは置いておいて、必要なのは分子と原子です。
原子量
原子は非常に微少なモノなので、質量そのものを言い表すと、10-24などになります。
このべき乗を直してみると、
1/1,000,000,000,000,000,000,000,000になり不便です。
そのため、炭素の同位体12Cを基準にして、相対的な数値で表そうと言うことになりました。それが原子量です。
分子量
分子に含まれる原子量の和が分子量です。
物質量
炭素原子12gに含まれる原子の数(6.02×1023)を基準として、これと同じ数の粒子(原子や分子)などを1mol(モル)と定めました。密度の計算などには欠かせません。
※ 物質量(mol)の計算が出題されることがあるかもしれません。
とりあえず、その式量にグラム単位をつけた質量が1molとなります。
例えば、H2Oは水素(1.008)が2つと酸素(16.00)が1つなので式量は18です。
(H×2)+O=(1×2)+16=18
したがって、物質量は18gが1molとなります。
二酸化炭素なら、CO2ですから、炭素(12.00)が1つと酸素(16.00)が2つなので式量は44です。
C+(O×2)=12+(16×2)=44
これはそのまま、単体や化合物、混合物の重さと考えても差し支えありません。(危険物の試験なら)
実際の試験問題では、まれに物質同士が反応したときの物質量を求める問題が出題されることも
ありますが、基本的にかけ算と足し算なので、慌てずに計算してください。
空気の分子量
空気よりも軽い気体または蒸気についての問題が出題されることがあります。
空気は様々な化合物からなる混合物であり、その平均分子量は約29です。
これよりも小さい数値の分子量であれば、空気よりも軽いということになります。
H2(水素)やHe(ヘリウム)などが有名な軽い気体です。都市ガスは平均分子量が16で空気よりも軽いですが、プロパンガスは平均分子量が44であり、空気よりも重いです。
また、第4類危険物(引火性液体)の蒸気はすべて空気よりも重いということも覚えておきましょう。
物質の化学的分類
 化学的に物質を分類すると左図のようになります。
化学的に物質を分類すると左図のようになります。
この区分は試験に出題される事があるのでよく覚えておきましょう。
化合物と混合物の分類は特に注意が必要です。
同素体
同じ炭素原子で出来ていながら組成が違い性質が異なる物質が存在するときはお互いを同素体と言います。
ダイヤモンド≒炭、 酸素≒オゾン、 黄リン≒赤リン
異性体
分子式が同じであっても分子の構造が異なり性質が異なる物質同士を異性体と言います。
エチルアルコール≒ジメチルエーテル
※ 同素体や異性体も試験には出題されやすいです。同素体と同位体の違いもさることながら、黄色マーカーを引いた物質を必ず覚えてください。
まとめ
- 物質の変化には2つの種類があり物理変化(簡単に元に戻る変化)と化学変化(簡単に元に戻らない変化)がある。
- 化学変化の例は、「鉄がさびた」「濃硫酸に紙をつけると黒く変色した」「ガソリンが燃えて二酸化炭素と水蒸気が出来た」「水を電気分解で水素と酸素に分けた」などがある。
- 原子量は炭素の同位体12Cを基準にして、相対的な数値で表そうと定めた。
- 物質量は炭素原子12gに含まれる原子の数(6.02×1023)を基準として、これと同じ数の粒子(原子や分子)などを1mol(モル)と定めた。
- 物質の化学的分類は試験によくでる。(戻って、もう一度確認しましょう)
- 同素体とは、同じ炭素原子で出来ていながら組成が違い性質が異なる物質同士のこと。
ダイヤモンド≒炭、 酸素≒オゾン、 黄リン≒赤リン - 異性体とは、分子式が同じであっても分子の構造が異なり性質が異なる物質同士のこと。
エチルアルコール≒ジメチルエーテル
ちょっとこのページは覚えることが多いですが、がんばってください。

